- ¿Por qué importa este estudio?
- Objetivo del estudio
- Diseño y metodología
- Población incluida
- Intervención y comparador
- Desenlaces evaluados
- Resultados principales
- Efectos fisiológicos y conductuales de la intervención
- Seguridad y adherencia
- Fortalezas
- Limitaciones
- ¿Qué significa esto para la práctica?
- Conclusión editorial
- Referencia
¿Por qué importa este estudio?
La reanimación hemodinámica en shock séptico sigue atrapada en una paradoja: todos aceptan que corregir la hipoperfusión importa, pero no está claro cuál es la mejor forma de hacerlo ni cómo individualizar líquidos, vasopresores e inotrópicos en tiempo real. Los grandes ensayos de estrategias uniformes, como más vs menos líquidos o metas más altas vs más bajas de presión arterial, no han resuelto el problema. Parte del obstáculo parece ser la heterogeneidad fisiopatológica del shock séptico: no todos los pacientes están predominantemente hipovolémicos, vasopléjicos o con disfunción cardíaca, y tratarlos como si fueran iguales probablemente diluye el beneficio de cualquier estrategia rígida.
En ese contexto, el tiempo de llenado capilar (CRT) ha ganado terreno como marcador clínico de hipoperfusión periférica y como posible objetivo de reanimación. El primer ANDROMEDA-SHOCK había sugerido que una estrategia guiada por CRT podía asociarse con recuperación más rápida de la disfunción orgánica, menor administración de fluidos y mayor probabilidad de supervivencia frente a una estrategia guiada por lactato. ANDROMEDA-SHOCK-2 intenta dar el siguiente paso: no solo usar el CRT como meta, sino integrarlo dentro de un algoritmo de reanimación hemodinámica verdaderamente personalizado.
Objetivo del estudio
El objetivo del ensayo fue determinar si una estrategia de reanimación hemodinámica personalizada dirigida a normalizar el tiempo de llenado capilar, denominada CRT-PHR, mejoraba un desenlace compuesto jerárquico de mortalidad, duración del soporte vital y duración de la estancia hospitalaria en comparación con el cuidado habitual en pacientes con shock séptico temprano.
Diseño y metodología
ANDROMEDA-SHOCK-2 fue un ensayo clínico aleatorizado, multicéntrico, abierto, realizado en 86 UCI de 19 países de América, Europa y Asia entre marzo de 2022 y abril de 2025, con último seguimiento en julio de 2025. Los pacientes fueron aleatorizados 1:1 a CRT-PHR o cuidado habitual, con estratificación por centro y bloques permutados de tamaño variable. La asignación se realizó mediante un sistema web con ocultamiento central de la secuencia. El estudio fue no cegado para clínicos y pacientes.
El desenlace primario fue un compuesto jerárquico a 28 días que incluyó, en este orden: mortalidad, duración del soporte vital y duración de la estancia hospitalaria. El análisis se hizo mediante win ratio estratificado por la mediana del APACHE II. En términos prácticos, cada paciente del grupo intervención se comparó con pacientes del grupo control dentro de su estrato; primero se definía “ganador” por mortalidad, y solo si ambos sobrevivían se pasaba a comparar duración del soporte vital y, después, estancia hospitalaria. Este diseño buscó capturar mejor la carga real de enfermedad que un análisis centrado únicamente en mortalidad.
Población incluida
Se consideraron elegibles adultos con shock séptico definido por infección sospechada o confirmada, hiperlactatemia de al menos 2.0 mmol/L y necesidad de norepinefrina para mantener una presión arterial media de al menos 65 mmHg tras una carga intravenosa mínima de 1000 mL. La inclusión debía ocurrir dentro de las primeras 4 horas desde que se cumplían estos criterios. Los pacientes podían identificarse en UCI, urgencias, quirófano o salas hospitalarias.
Se aleatorizaron 1501 pacientes y 1467 quedaron en el análisis primario: 720 en el grupo CRT-PHR y 747 en el grupo de cuidado habitual. La edad media fue de 66 años y 43.3% eran mujeres. La gravedad basal fue comparable, con APACHE II mediano de 19 vs 18 y SOFA mediano de 8 en ambos grupos. Cerca del 60% de los pacientes tenían CRT anormal al inicio, y la fuente infecciosa más frecuente fue abdominal, seguida de respiratoria y urinaria. El tiempo desde cumplir criterios de shock séptico hasta la aleatorización fue corto, con mediana de 2 horas en ambos grupos.
| Característica | Grupo CRT-PHR (n = 720) | Grupo de cuidado habitual (n = 747) |
|---|---|---|
| Edad, mediana (RIC), años | 66.0 (52.0-74.0) | 65.0 (51.0-76.0) |
| Sexo, n (%) | ||
| Femenino | 302 (41.9) | 334 (44.7) |
| Masculino | 418 (58.1) | 413 (55.3) |
| Peso, mediana (RIC) [n total], kg | 70.0 (60.0-80.0) [n = 717] | 70.0 (60.4-80.0) [n = 747] |
| Puntajes de severidad, mediana (RIC) | ||
| APACHE II | 19.0 (14.0-24.0) | 18.0 (13.0-23.0) |
| SOFA [n total] | 8.0 (7.0-11.0) [n = 719] | 8.0 (7.0-10.0) [n = 745] |
| Índice de comorbilidad de Charlson | 4.0 (2.0-5.0) | 3.0 (2.0-5.0) |
| Comorbilidades | ||
| Hipertensión crónica | 162/705 (23.0) | 179/730 (24.5) |
| Diabetes | 167/706 (23.7) | 161/731 (22.0) |
| Enfermedad pulmonar crónica | 81/703 (11.5) | 65/730 (8.9) |
| Diabetes con complicaciones crónicas | 58/701 (8.3) | 47/726 (6.5) |
| Cáncer no hematológico | 46/702 (6.6) | 30/727 (4.1) |
| Cáncer hematológico | 12/700 (1.7) | 21/726 (2.9) |
| Fuente de la infección | ||
| Abdominal | 350/717 (48.8) | 343/745 (46.0) |
| Respiratoria | 126/717 (17.6) | 156/745 (20.9) |
| Urinaria | 151/717 (21.1) | 131/745 (17.6) |
| Cutánea y tejidos blandos | 42/717 (5.9) | 55/745 (7.4) |
| Torrente sanguíneo | 27/717 (3.8) | 39/745 (5.2) |
| Ósea y articular | 5/717 (0.7) | 7/745 (0.9) |
| Sistema nervioso central | 6/717 (0.8) | 5/745 (0.7) |
| Mediastinitis | 6/717 (0.8) | 4/745 (0.5) |
| Otras | 4/717 (0.6) | 5/745 (0.7) |
| Infección confirmada microbiológicamente | 454/707 (64.2) | 470/741 (63.4) |
| Tiempo desde cumplir criterios de choque séptico hasta la aleatorización, mediana (RIC), h | 2 (1-3) | 2 (1-3) |
| Soporte orgánico al inicio | ||
| Respiratorio | ||
| Ninguno | 82/719 (11.4) | 93/741 (12.6) |
| Oxígeno de bajo flujo | 221/719 (30.7) | 213/741 (28.7) |
| Cánula nasal de alto flujo | 56/719 (7.8) | 52/741 (7.0) |
| Ventilación mecánica no invasiva | 23/719 (3.2) | 18/741 (2.4) |
| Ventilación mecánica invasiva | 337/719 (46.9) | 365/741 (49.3) |
| Cardiovascular | ||
| Norepinefrina | 720/720 (100.0) | 747/747 (100.0) |
| Vasopresina | 166/701 (23.7) | 149/726 (20.5) |
| Epinefrina | 8/700 (1.1) | 13/726 (1.8) |
| Dobutamina | 8/701 (1.1) | 5/726 (0.7) |
| Otros | 1/701 (0.1) | 2/726 (0.3) |
| Variables hemodinámicas y de perfusión | ||
| Carga intravenosa de líquidos, mediana (RIC), mL | 1500 (1000-2000) | 1500 (1000-2000) |
| Carga intravenosa de líquidos por peso, mediana (RIC), mL/kg | 22.1 (14.3-30.8) | 21.4 (14.7-30.4) |
| Presión arterial media, mediana (RIC), mm Hg | 69 (64-76) | 69 (65-76) |
| Frecuencia cardíaca, mediana (RIC), latidos/min | 102 (89-116) | 105 (89-117) |
| Dosis de norepinefrina, mediana (RIC), μg/kg/min | 0.23 (0.12-0.40) | 0.21 (0.10-0.39) |
| Lactato sérico, mediana (RIC), mmol/L | 3.7 (2.7-5.5) | 3.6 (2.7-5.3) |
| Lactato sérico >4.0 mmol/L, n (%) | 315 (43.8) | 314 (42.0) |
| Tiempo de llenado capilar, mediana (RIC) [n total], s | 4.0 (2.4-5.7) [n = 719] | 4.0 (3.0-6.0) [n = 742] |
| Tiempo de llenado capilar >3 s, n (%) | 419/719 (58.3) | 459/742 (61.9) |
| Diferencia venoarterial de dióxido de carbono, mediana (RIC) [n total], mm Hg | 6.8 (4.4-9.0) [n = 620] | 6.3 (4.1-9.0) [n = 616] |
| Diferencia venoarterial de dióxido de carbono >6 mm Hg | 324/620 (52.3) | 314/616 (51.0) |
| Saturación venosa central de oxígeno, mediana (RIC) [n total], % | 74 (67-81) [n = 626] | 73 (66-79) [n = 630] |
| Saturación venosa central de oxígeno <75% | 330/626 (52.7) | 362/630 (57.5) |
Abreviaturas: APACHE = Acute Physiology and Chronic Health Evaluation; CRT-PHR = resucitación hemodinámica personalizada guiada por tiempo de llenado capilar; SOFA = Sequential Organ Failure Assessment.
Intervención y comparador
La estrategia CRT-PHR se ejecutó durante un período de estudio de 6 horas y tuvo como meta normalizar el CRT, definido como un llenado capilar >3 segundos cuando era anormal. La evaluación se estandarizó con presión sobre la falange distal mediante una lámina de vidrio durante 10 segundos, midiendo luego el tiempo hasta el retorno del color normal con cronómetro.
El algoritmo, resumido visualmente en el diagrama de la página 4, se organizó en dos niveles progresivos. En el tier 1, si la presión de pulso era menor de 40 mmHg, se evaluaba respuesta a liquídos y, si era positiva, se administraban bolos de 500 mL hasta un máximo de 1000 mL. Si la presión de pulso era de al menos 40 mmHg pero la presión diastólica era menor de 50 mmHg, se titulaba norepinefrina para elevar la presión diastólica por encima de 50 mmHg. Si el CRT seguía anormal, se avanzaba al tier 2: ecocardiografía básica para descartar disfunción ventricular, nueva evaluación de respuesta a líquidos, prueba transitoria de mayor presión arterial media en hipertensos crónicos y, si persistía la alteración, una prueba de dobutamina a dosis fija de 5 μg/kg/min durante 1 hora.
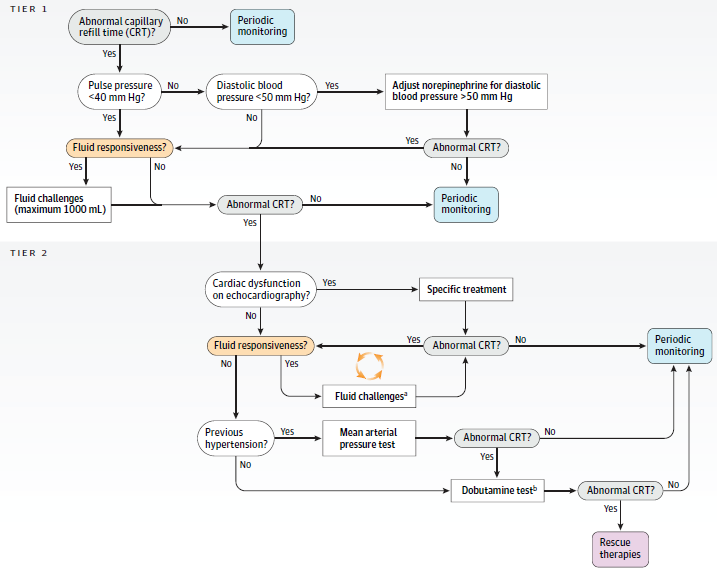
El grupo control recibió cuidado habitual según protocolos locales o guías internacionales. Se permitían ecocardiografía y evaluación de respuesta a líquidos, pero no eran obligatorias. El CRT solo se medía al inicio y a las 6 horas. Ese punto es importante: el comparador no fue un grupo “ciego” o pasivo, sino una práctica habitual bastante activa.
Desenlaces evaluados
El desenlace primario fue el compuesto jerárquico de mortalidad a 28 días, duración del soporte vital y duración de la estancia hospitalaria. La duración del soporte vital incluía el tiempo hasta el cese de vasopresores, ventilación mecánica y terapia de reemplazo renal. Si un paciente reiniciaba alguno de estos soportes, se tomaba el final del último período de soporte.
Los desenlaces secundarios, analizados en secuencia jerárquica, fueron mortalidad por cualquier causa a 28 días, días libres de soporte vital dentro de 28 días y duración de la estancia hospitalaria hasta el día 28. También hubo desenlaces terciarios y subgrupos presentados en el suplemento.
Resultados principales
El ensayo fue positivo para el desenlace primario. A los 28 días, el grupo CRT-PHR acumuló 131 131 wins (48.9%) frente a 112 787 (42.1%) en el grupo de cuidado habitual, con un win ratio estratificado de 1.16 (IC 95% 1.02 a 1.33; p=0.04). El componente que más contribuyó a esta superioridad fue la menor duración del soporte vital. Los wins individuales fueron 19.1% vs 17.8% para muerte, 26.4% vs 21.1% para duración del soporte vital y 3.4% vs 3.2% para estancia hospitalaria, a favor de la intervención frente al cuidado habitual. La figura de la página 8 (a continuación la dejamos) muestra que el efecto fue consistente en ambos estratos de APACHE II, aunque más sólido en el estrato de mayor gravedad.
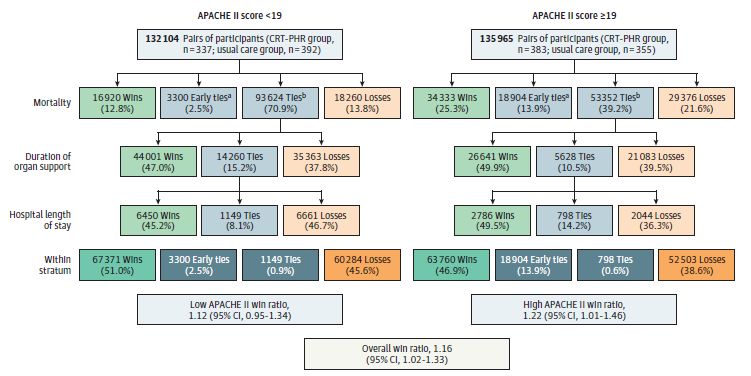
| Variable | Grupo CRT-PHR | Grupo de cuidado habitual | Diferencia absoluta (IC 95%) |
|---|---|---|---|
| Terapia | |||
| Norepinefrina, n/n total (%) | 648/684 (94.7) | 634/694 (91.4) | 3.4 (0.7 a 6.1) |
| Dosis de norepinefrina, media (DE), μg/kg/min | 0.28 (0.34) [n = 655] | 0.27 (0.41) [n = 634] | −0.01 (−0.05 a 0.03) |
| Vasopresina, n/n total (%) | 251/684 (36.7) | 229/694 (33.0) | 3.7 (−1.3 a 8.7) |
| Dobutamina, n/n total (%) | 84/684 (12.3) | 37/694 (5.3) | 7.0 (4.0 a 9.9) |
| Volumen de fluidos de reanimación, media (DE), mL | 595 (679) [n = 672] | 847 (832) [n = 676] | −251 (−316 a −187) |
| Balance hídrico neto, media (DE), mL | 990 (1016) [n = 629] | 1227 (1225) [n = 622] | −242 (−385 a −99) |
| Variables hemodinámicas y de perfusión | |||
| Presión venosa central, media (DE), mm Hg | 9.1 (4.1) [n = 541] | 9.8 (4.8) [n = 544] | −0.6 (−1.1 a −0.1) |
| Presión arterial media, media (DE), mm Hg | 74.1 (9.4) [n = 682] | 73.6 (9.0) [n = 690] | 0.6 (−0.5 a 1.7) |
| Tiempo de llenado capilar, media (DE), s | 2.8 (1.4) [n = 679] | 3.4 (1.9) [n = 684] | −0.6 (−0.7 a −0.4) |
| Lactato, media (DE), mmol/L | 3.2 (2.4) [n = 659] | 3.5 (3.0) [n = 664] | −0.3 (−0.5 a −0.1) |
| Saturación venosa central de oxígeno, media (DE), % | 74.4 (8.9) [n = 588] | 72.4 (9.9) [n = 596] | 1.9 (0.8 a 3.0) |
Abreviatura: CRT-PHR = resucitación hemodinámica personalizada guiada por tiempo de llenado capilar.
Sin embargo, la mortalidad aislada a 28 días no cambió: 26.5% en CRT-PHR frente a 26.6% en cuidado habitual, con HR de 0.99 (IC 95% 0.81 a 1.21; p=0.91). Los pacientes del grupo intervención tuvieron más días libres de soporte vital dentro de 28 días, con media de 16.5 vs 15.4 días y una OR 1.28 (IC 95% 1.06 a 1.54). La estancia hospitalaria fue numéricamente menor, 15.3 vs 16.2 días, pero sin una diferencia claramente concluyente.
Efectos fisiológicos y conductuales de la intervención
Durante las primeras 6 horas, el grupo CRT-PHR logró normalizar el llenado capilar con mayor frecuencia que el cuidado habitual: 85.9% vs 61.7%. Además, recibió menos líquidos de resucitación, 595 mL frente a 847 mL, con una diferencia media de −251 mL. También tuvo menor balance neto, menor presión venosa central, menor lactato y menor CRT a las 6 horas. En contraste, recibió más dobutamina, 12.3% vs 5.3%.
Hay un hallazgo especialmente interesante: 36.4% de los pacientes del grupo intervención comenzaron y permanecieron con CRT normal durante todo el período de estudio, por lo que no recibieron nuevas intervenciones hemodinámicas. Eso sugiere que el algoritmo no solo sirve para “hacer más cosas”, sino también para identificar a quién no seguir reanimando agresivamente. Ese punto tiene peso clínico real, porque una estrategia de personalización útil no es la que siempre intensifica el tratamiento, sino la que evita tanto el infra como el sobretratamiento.
| Desenlace | Grupo CRT-PHR (n = 720) | Grupo de cuidado habitual (n = 747) | Estimador de efecto (IC 95%) | Valor p |
|---|---|---|---|---|
| Desenlace primario hasta 28 días | ||||
| Compuesto jerárquico de muerte, duración del soporte vital y estancia hospitalaria | 131 131 (48.9) | 112 787 (42.1) | SWR, 1.16 (1.02 a 1.33) | .04 |
| Desenlaces secundarios | ||||
| Mortalidad por cualquier causa a 28 días | 191 (26.5) | 199 (26.6) | HR, 0.99 (0.81 a 1.21) | .91 |
| Días libres de soporte vital dentro de 28 días | ||||
| Media (DE) | 16.5 (11.3) | 15.4 (11.4) | pOR, 1.28 (1.06 a 1.54) | NA |
| Mediana (RIC) | 23.0 (0 a 25.0) | 22.0 (0 a 25.0) | ||
| Estancia hospitalaria hasta el día 28, d | ||||
| Media (DE) | 15.3 (9.0) | 16.2 (9.4) | MD, −0.85 (−1.80 a 0.10) | NA |
| Mediana (RIC) | 13.0 (8.0 a 25.0) | 15.0 (8.0 a 28.0) | ||
Abreviaturas: CRT-PHR = resucitación hemodinámica personalizada guiada por tiempo de llenado capilar; HR = hazard ratio; MD = diferencia media; NA = no aplica; pOR = proportional odds ratio; SWR = stratified win ratio.
Seguridad y adherencia
La adherencia al protocolo fue razonablemente alta. En el grupo CRT-PHR hubo desviaciones en 15% y violaciones de protocolo en 6%. Algunas pruebas se omitieron por consideraciones de seguridad previamente definidas, y solo una prueba de dobutamina se suspendió por hipotensión, la cual revirtió al suspender el fármaco. Se reportaron cinco sospechas de reacciones adversas serias inesperadas, sin diferencias entre grupos, y ninguna se consideró probablemente relacionada con el protocolo.
Fortalezas
ANDROMEDA-SHOCK-2 tiene varias fortalezas reales. Es un ensayo grande para el contexto de shock séptico, internacional, multicéntrico y diseñado para intervenir muy temprano, dentro de las primeras 4 horas. La intervención fue explícitamente protocolizada, entrenable y auditable, lo cual importa mucho cuando se estudian estrategias complejas y no un solo fármaco. Además, el estudio no comparó la estrategia contra una caricatura de “mala práctica”, sino contra un cuidado habitual bastante sofisticado, donde 62% de los pacientes tuvo evaluación de respuesta a líquidos y 68% ecocardiografía básica. Eso hace más exigente la comparación.
Otra fortaleza es conceptual: el algoritmo integra fisiología clínica simple con decisiones escalonadas. El estudio no propone que el CRT reemplace todo, sino que funcione como puerta de entrada a una reanimación más específica. La figura Algoritmo de reanimación hemodinámica personalizada por CRT (CRT-PHR) resume bien esa lógica por capas: primero patrones simples y acciones rápidas; después ecocardiografía, prueba de MAP y dobutamina solo si persiste la alteración. Es una estrategia más pragmática que tecnocrática.
Limitaciones
La principal limitación es que el ensayo fue abierto. Y aquí eso importa más de lo habitual, porque el componente que “ganó” el estudio no fue la mortalidad, sino la duración del soporte vital. Decisiones como retirar vasopresores, extubar o iniciar y suspender terapia de reemplazo renal no fueron adjudicadas centralmente y quedaron a criterio de los intensivistas locales. Los autores argumentan que eso debería generar ruido aleatorio y no sesgo sistemático, pero esa defensa no elimina por completo la inquietud. Si el resultado positivo depende sobre todo de un desenlace más sensible a la conducta clínica, el no cegamiento pesa.
También hay limitaciones de implementación. El CRT puede estar sujeto a variabilidad interobservador. Los puntos de corte propuestos para presión de pulso y presión diastólica parecen fisiológicamente razonables, pero no tenían validación clínica prospectiva previa. Además, aunque el protocolo resultó factible, sigue siendo más laborioso que una conducta menos estructurada, y no puede descartarse que parte del efecto provenga simplemente de que el grupo intervención fue evaluado con más frecuencia y más disciplina.
Hay otra crítica importante: el ensayo fue positivo para un desenlace compuesto jerárquico, pero no para mortalidad aislada. Eso no invalida el hallazgo, pero sí obliga a una lectura más sobria. El mensaje correcto no es “CRT-PHR salva más vidas”, porque el estudio no mostró eso. El mensaje es más acotado: la estrategia se asoció con mejor desempeño en un compuesto centrado sobre todo en menor duración del soporte vital. Eso es clínicamente valioso, pero no es lo mismo que reducir muerte.
¿Qué significa esto para la práctica?
Este ensayo respalda bastante bien una idea que muchos clínicos ya intuían, pero que hasta ahora tenía soporte incompleto: en shock séptico temprano, una reanimación hemodinámica guiada por signos clínicos de perfusión y personalizada según el patrón hemodinámico puede ser mejor que seguir acumulando líquidos o decisiones inespecíficas. El grupo CRT-PHR normalizó más rápido el CRT, recibió menos líquidos, tuvo menor lactato a las 6 horas y terminó con menos tiempo de soporte vital. Eso sugiere una reanimación más eficiente y probablemente menos iatrogénica.
Pero tampoco conviene sobreactuar. ANDROMEDA-SHOCK-2 no demuestra que el CRT por sí solo sea “la” solución ni que cualquier protocolo con CRT sea superior. Lo que funcionó aquí fue un algoritmo completo, con entrenamiento, evaluación secuencial, pruebas reversibles y escalamiento racional. Reducir el mensaje a “mida CRT y ya” sería banalizar el estudio. De hecho, buena parte de la plausibilidad del beneficio está en que el protocolo evitó líquidos innecesarios en algunos y promovió vasopresores, inotrópicos o evaluación cardíaca en otros.
CIEMER
Conclusión editorial
ANDROMEDA-SHOCK-2 no es el ensayo que “por fin resolvió” la reanimación del shock séptico. No mostró menos mortalidad y su desenlace positivo depende principalmente de menos tiempo en soporte vital. Pero sería un error minimizarlo por eso. Lo que aporta es algo más útil y probablemente más cercano a la práctica real: demuestra que una reanimación temprana, estructurada y personalizada alrededor del CRT puede ordenar mejor las decisiones y evitar tanto el automatismo de los líquidos como la ceguera fisiológica del manejo estándar.
El mensaje práctico no es que el CRT reemplace al juicio clínico, al ecógrafo o a la monitorización hemodinámica. El mensaje es más exigente: dejar de reanimar a todos igual. Si algo hace valioso a este ensayo es que devuelve el foco a una medicina crítica menos ritual y más dirigida por la fisiología al lado de la cama. Eso merece atención. Pero no licencia triunfalismo: antes de vender CRT-PHR como nuevo estándar incuestionable, todavía hay que probar cuánto del efecto es reproducible fuera del entorno protocolizado y cuánto depende de equipos entrenados y altamente adherentes.
CIEMER
Referencia
The ANDROMEDA-SHOCK-2 Investigators for the ANDROMEDA Research Network, Spanish Society of Anesthesiology, Reanimation and Pain Therapy (SEDAR), and Latin American Intensive Care Network (LIVEN). Personalized Hemodynamic Resuscitation Targeting Capillary Refill Time in Early Septic Shock: The ANDROMEDA-SHOCK-2 Randomized Clinical Trial. JAMA. 2025;334(22):1988–1999. doi:10.1001/jama.2025.20402
CIEMER
Especialista en medicina de emergencias
Fellow de medicina crítica y cuidado intensivo
MsC en educación para profesionales de la salud
Master en toxicología
CEO CIEMER S.A.S






Deja una respuesta