Introducción
- El potasio (K+) es un catión esencial para la función celular, y los niveles de K+ en suero los regula el cuerpo en un rango estrecho (de 3.5 a 5.0 mmol/l).
- La hiperK se refiere a un aumento en la concentración de K+, aunque no existe una definición universal.
- Comúnmente se define como una concentración de K+ sérico (sK+) ≥ 5.0 mmol/l, aunque este límite puede variar dependiendo de los laboratorios individuales y difiere entre las mediciones en plasma y suero; y de la bibliografía disponible donde algunos autores toman como punto de corte 5.5 mmol/l.
- No hay una definición común y estandarizada para la clasificación de la severidad de la hiperK (como leve, moderada o severa). Las concentraciones de K+ varían dependiendo de si se analizó el K+ en suero o plasma, con las concentraciones en suero usualmente más altas que las del plasma.
- La hiperK es un problema de importancia clínica para pacientes y médicos, debido, en parte, a sus consecuencias clínicas reconocidas desde hace tiempo, incluyendo arritmias cardiacas.
- El verdadero impacto epidemiológico de la hiperK ha sido aún mejor caracterizado; un nivel elevado de K+ está asociado con la hospitalización, mortalidad y grandes incrementos en los costos de atención en salud a nivel poblacional.
- Existe una fuerte asociación entre los inhibidores del Sistema Renina-Angiotensina-Aldosterona (SRAAi), a saber, los Inhibidores de la Enzima Convertidora de Angiotensina (IECAs), los Antagonistas de los Receptores de Angiotensina (ARA) y los Antagonistas de los Receptores de Mineralocorticoides (ARM), y la hiperK.
- Los SRAAi son un pilar clave de la terapia para enfermedades renales, diabetes e insuficiencia cardíaca. Por lo tanto, suspender estos medicamentos en respuesta a la hiperK compromete la atención y puede, a su vez, conducir a morbilidad y mortalidad.
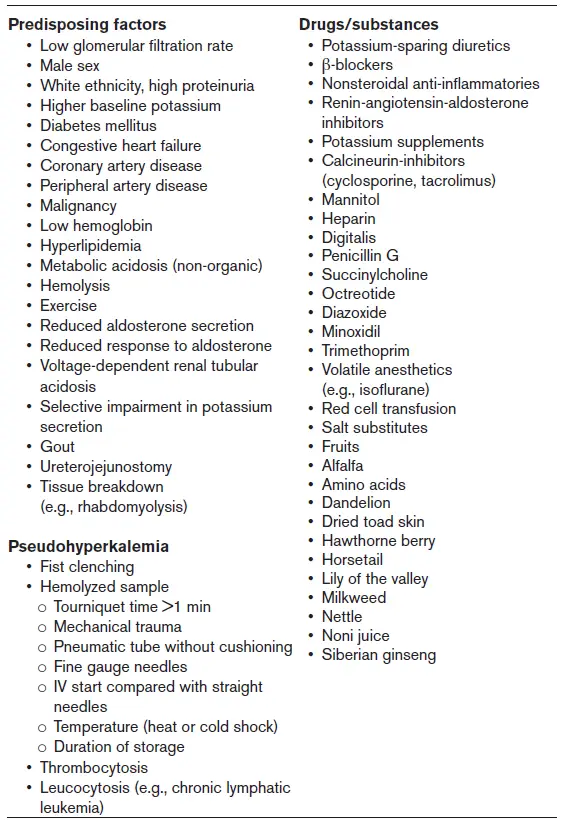
- La PseudohiperK es una concentración elevada falsamente de K+ en suero, que puede ocurrir por varios motivos, como trauma mecánico, uso prolongado de torniquete (>1 minuto) o apretar el puño durante el proceso de extracción de sangre, coagulación sanguínea, centrifugación, aumento en el conteo de células blancas o trombocitosis.
Epidemiología
- Población General:
- La prevalencia descrita es del 1.5% para concentraciones de K+ ≥5 mmol/l.
- Aumenta hasta el 5.6% en pacientes que recientemente comenzaron tratamiento con IECAs o ARA.
- Diferentes umbrales de K+ afectan la incidencia reportada de la hiperK, lo que hace variar la estadística.
- La incidencia mundial de hiperK podría ser subestimada debido a la falta de monitoreo rutinario de K+, especialmente en poblaciones de pacientes de alto riesgo.
- Pacientes hospitalizados:
- Incidencia de hiperK de 3.5% (>5.5 mEq/L) en Canadá y 4.9% (>5.0 mEq/L) en Irlanda.
- Pacientes con Insuficiencia Cardíaca:
- En aquellos de clase III y IV de la New York Heart Association (NYHA), con una fracción de eyección del ventrículo izquierdo (FEVI) <35% y recién medicados con espironolactona, la prevalencia puntual fue del 19%, comparada con un 5.6% en pacientes asignados a placebo.
- Servicio de Urgencias (SU):
- 8% en un SU suizo (definido como sK+ >4.7 mmol/l).
- 6% en un SU de EE. UU. (definido como sK+ >5 mmol/l).
- 3% de los pacientes en el SU de un hospital universitario suizo presentaron hiperK definida como concentraciones de K+ en suero o plasma ≥6 mmol/l.
- Injuria Renal Aguda (IRA) en la UCI:
- La prevalencia fue del 3.4% sin IRA.
- 8% en IRA etapa 1.
- 17% en IRA etapa 2.
- 2% en IRA etapa 3.
- Enfermedad Renal Crónica (ERC):
- 8% en una gran cohorte de EE. UU. con una tasa de filtración glomerular estimada (TFGe) <30 ml/min/1.73 m2.
- 4–5% en una cohorte italiana con la misma condición.
Clasificación
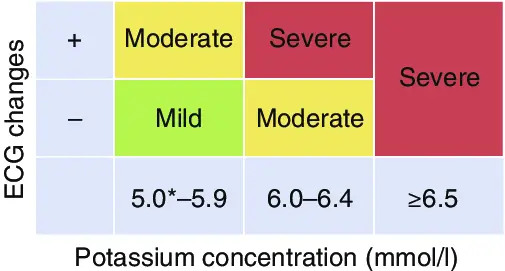
- La clasificación de la hiperK aguda debe considerar tanto el nivel absoluto en suero como la presencia o ausencia de cambios en el electrocardiograma (ECG) consistentes con hiperK.
- Se clasifica desde leve (sK+ 5.0–5.9 mmol/l sin cambios en el ECG) hasta severa (sK+ ≥6.0 mmol/l con cambios en el ECG o ≥6.5 mmol/l independientemente de los hallazgos del ECG).
Homeostasis
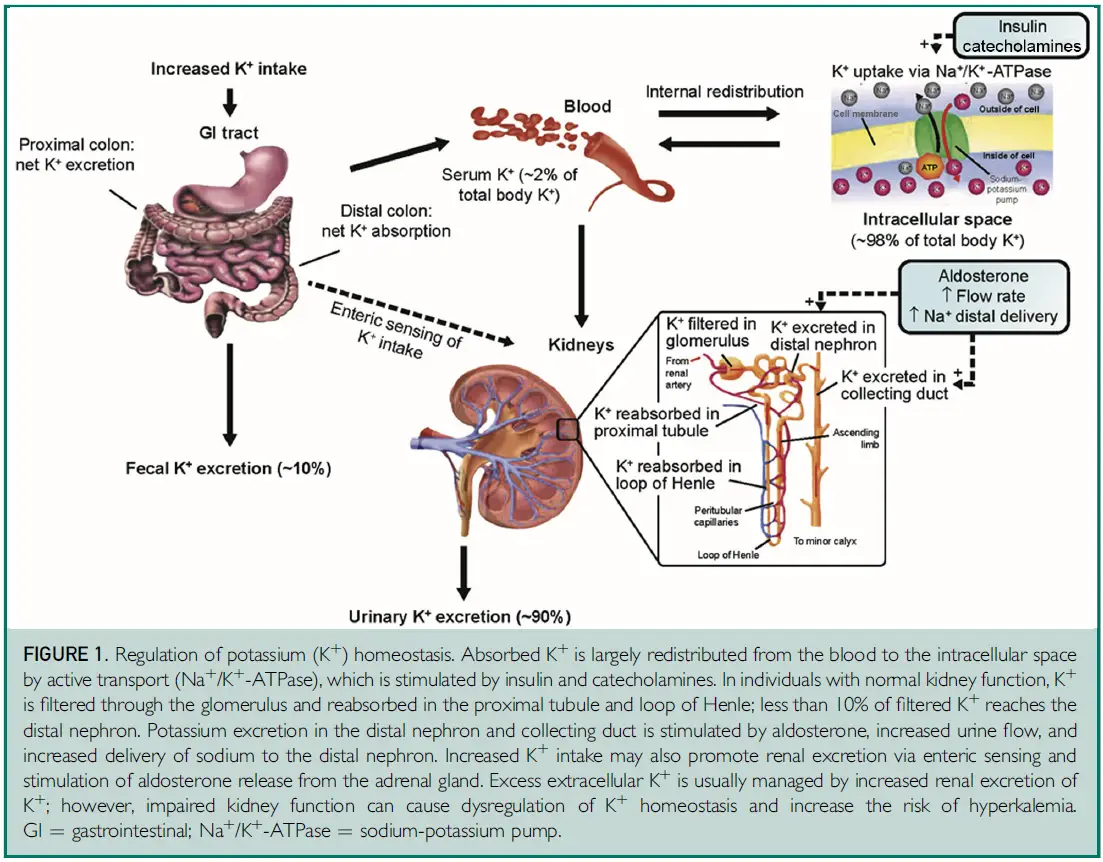
- Mantenimiento de la homeostasis del K+:
- Principalmente mantenida por los riñones, aunque el tracto gastrointestinal y otros sistemas también están involucrados en menor medida.
- Efectos de la hiperK:
- Tiene efectos despolarizantes en el corazón, causando potenciales de acción acortados y aumentando el riesgo de arritmias.
- Causa síntomas neuromusculares, acidosis metabólica y supresión de la amoniogénesis.
- Incrementa el riesgo de mortalidad, morbilidad cardiovascular, progresión de la enfermedad renal crónica (ERC), y hospitalización, especialmente en pacientes con ERC, insuficiencia cardíaca (IC), y diabetes tipo 2 (DM).
- Relación entre Sk+ y mortalidad:
- Existe una curva en forma U entre las concentraciones sK+ y la mortalidad, tanto la hiperK como la hipoK están asociadas con resultados clínicos adversos.
- La concentración exacta de K+ considerada potencialmente letal sigue siendo controversial.
- Variabilidad del riesgo de hiperK:
- El riesgo de hiperK y el rango óptimo para las concentraciones de sK+ varían según las comorbilidades individuales del paciente, como ERC, IC o DM.
- Tolerancia a la hiperK en ERC:
- En pacientes con ERC, mecanismos compensatorios pueden resultar en tolerancia a elevadas concentraciones circulantes de K+.
- Varios estudios han sugerido que la hiperK es una condición menos amenazante en ERC.
- Un estudio retrospectivo encontró una asociación más fuerte entre hiperK y mortalidad a 1 día en pacientes con función renal normal en comparación con aquellos con ERC.
- Estudios sobre hiperK y mortalidad en ERC:
- Se observó una disminución gradual en el riesgo de mortalidad a medida que el estadio de ERC empeoraba en hospitalizaciones por hiperK severa.
- Un estudio de cohorte mostró un menor riesgo de mortalidad pre-Enfermedad Renal Terminal (ESRD por sus siglas en inglés) cuando las concentraciones de sK+ estaban entre 4.0 a 5.5 mmol/l.
- Adaptaciones a la hiperk:
- Se sugiere que los pacientes con ERC se adaptan a concentraciones elevadas de K+ a través de modificaciones en las secreciones de K+ gastrointestinal y aumentando la captación intracelular de K+ mediada por insulina.
- Se desconoce si estas adaptaciones existen en otras células, como los cardiomiocitos.
- Canales de K+ y riesgo mortalidad:
- Los canales de K+ en el miocardio son sensibles a cambios en factores endógenos y pueden cambiar en número o funcionamiento en respuesta a alteraciones estructurales y ambientales.
- Futuros estudios deberían investigar si estos cambios pueden explicar las reducciones observadas en el riesgo relativo de muerte por hiperK en pacientes con ERC avanzada.
Etiología y factores de riesgo
- Pacientes en etapas avanzadas de ERC, IC, DM, infarto de miocardio (IM), y/o combinaciones de estas condiciones tienen un riesgo aumentado de morbilidad y mortalidad asociadas a la hiperK.
- Son factores de riesgo adicionales: uso de SRAAi, edad avanzada, y medicamentos como heparina, beta-bloqueantes, antiinflamatorios no esteroideos (AINES), inhibidores de calcineurina, trimetoprima, pentamidina, y diuréticos ahorradores de K.
- En pacientes con ERC el riesgo de hiperK aumenta progresivamente a medida que disminuye la TFGe. El riesgo generalmente se incrementa una vez que la TFGe < 15 mL/min por 1.73 m².
- En pacientes que reciben SRAAi con una TFGe <60 mL/min por 1.73 m² tienen un riesgo elevado de hiperK, el cual aumenta progresivamente a medida que disminuye la TFGe.
- Los pacientes con riesgo de hiperK recurrente incluyen hiperK inicial moderada a severa (≥5.6 mEq/L), baja TFGe (<45 mL/min por 1.73 m²), DM y uso de espironolactona.
- El riesgo de hiperK es ligeramente mayor en hombres que en mujeres después de iniciar terapia con SRAAi y varía entre grupos raciales, donde la etnicidad, dieta y factores socioeconómicos pueden contribuir.
- La dieta baja en K+ se recomienda en pacientes con ERC en etapa avanzada para reducir el riesgo de hiperK. Sin embargo, la evidencia existente no es fuerte.
Signos y síntomas
Aunque muchos pacientes son asintomáticos, la hiperK puede manifestarse clínicamente con debilidad muscular, parestesias y fasciculaciones musculares en brazos y piernas como señales tempranas. La parálisis, anomalías de la conducción cardíaca y arritmias cardíacas pueden ser letales.
Debilidad muscular
- Suele ser ascendente, comenzando en las piernas y progresando hacia el tronco, a veces asemejándose al síndrome de Guillain–Barré.
Alteraciones cardíacas
- Causadas por sus efectos despolarizantes en las células musculares cardíacas y suelen ser progresivas.
- Una revisión reciente sugirió que la presencia y naturaleza de los cambios en el ECG, junto con la concentración absoluta de K+, pueden usarse como pronosticadores de resultado.
- Uno de los estudios más grandes y recientes sobre los cambios en el ECG en pacientes con hiperK, que incluyó un total de 90 pacientes, reportó que el ECG es insensible para la detección de hiperK y no encontró correlación entre la presencia de cambios en la onda T y la concentración de K en suero.
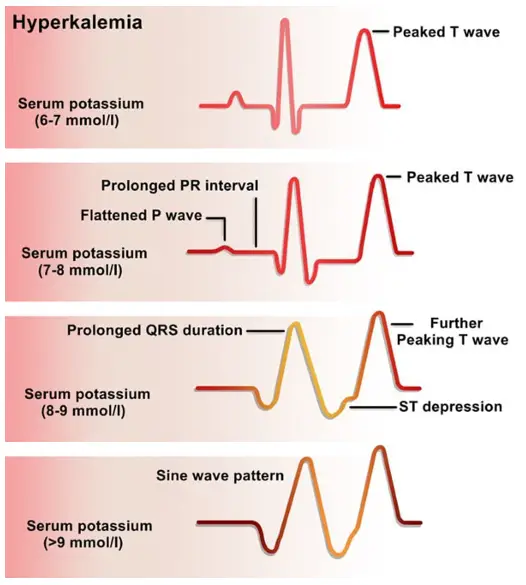
- Las ondas T altas y picudas pueden ser, sin embargo, signos tempranos de hiperK en el ECG.
Cambios típicos en el ECG
- Disminución de la amplitud de la onda P.
- Intervalo PR prolongado.
- Ensanchamiento del complejo QRS.
- El patrón clásico que ocurre con un ensanchamiento más severo del QRS y fusión del complejo QRS con segmentos ST-T ensanchados, es el patrón de onda sinusoidal.
- Los cambios en el ECG son conocidos por asemejarse a un IAM con elevación del ST o al Síndrome de Brugada en algunos casos.
- Es importante destacar que hasta la mitad de los pacientes con hiperK tienen un ECG normal, incluidos algunos pacientes con hiperK extrema.
- Reconocer la falta de sensibilidad del ECG convencional para el diagnóstico es importante en la práctica clínica.
Diagnóstico
- En muchos casos en el servicio de urgencias el diagnóstico de la hiperK es incidental mediante medición de electrolitos séricos.
- En pacientes sin factores de riesgo para hiperK, o cuando el hallazgo de hiperK no parece plausible, se debe considerar la pseudohiperkalemia.
- Point Of Care (PoC)
- Los PoC resultaron suficientemente precisos con diferencias medias entre 0.1 y 0.5 mmol/l comparado con la medición de laboratorio central.
- Sin embargo, los PoC que analizan sangre total no pueden identificar la hemólisis, la cual puede resultar en una hiperK falsa.
- Los PoC deberían considerarse en pacientes en quienes se sospecha clínicamente hiperK basada en síntomas o ECG, y en aquellos con alto riesgo de hiperK (e.g., pacientes que se encuentran en diálisis).
- La disponibilidad rápida de resultados puede permitir un inicio más rápido del tratamiento.
- Se recomienda un ECG para evaluar la presencia de cambios en el ECG inducidos por hiperK.
- Además, se deben realizar pasos adicionales para clarificar la etiología de la hiperK.
- Estos pueden incluir una evaluación cuidadosa de la historia y medicaciones del paciente, detección de hemólisis, evaluación de la función renal y, si aplica, investigación de la causa de la injuria renal aguda (IRA).
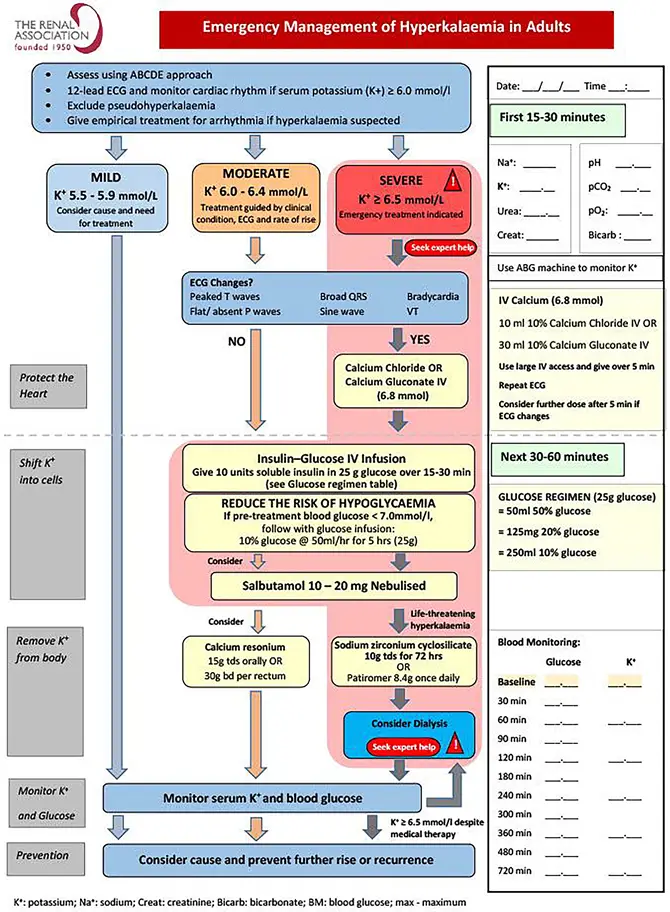
Tratamiento de la hiperK aguda
- El manejo de la hiperK aguda depende de la magnitud o severidad del aumento en la concentración de K+, especialmente cuando se combina con cambios en el ECG y debilidad muscular severa.
- El estudio REVEAL-ED mostró que los síntomas >5.5 mmol/l pueden ser inespecíficos y los hallazgos en el ECG pueden ser muy variables.
- Los estudios de alta calidad sobre el manejo de la hiperK aguda son escasos.
- Hasta la fecha no existe una guía internacional específica que trate el manejo de la hiperK.
- Todas las guías concuerdan que el tratamiento de la hiperK aguda debe corresponder a 3 objetivos específicos:
🎯Estabilización de la membrana celular
- Se realiza con la administración de sales de calcio por vía intravenosa.
- Están indicadas cuando hay cambios en el ECG sugestivas de hiperK.
- Se dispone de dos tipos:
- Cloruro de calcio:
- Mayor biodisponibilidad.
- concentración de calcio tres veces más que el gluconato.
- Dosis: 10 ml al 10% cada 5 a 10 minutos
- Requiere una vía central para su administración.
- Gluconato de calcio:
- Menor toxicidad tisular
- Dosis: 30 ml al 10% cada 5 a 10 minutos
- Se puede administrar por vía periférica
- Previene la fibrilación/taquicardia ventricular estabilizando la membrana celular cardíaca y es efectivo en 1–3 minutos tras la administración.
- Indicación: A todos los pacientes con concentración de K+ >6.5 mmol/l y cambios en el ECG o con imposibilidad de obtener un ECG o monitorización inmediata.
- La hipercalcemia inducida en estos pacientes no ha demostrado peores resultados.
- La administración de sales de calcio NO reduce la concentración de K+ y su duración de acción está limitada a 30–60 minutos.
- Cloruro de calcio:
🎯Desplazamiento del K al compartimento intracelular
- Se deben implementar medidas para trasladar el potasio del compartimiento extracelular al intracelular. Éstas incluyen:
- Insulina:
- Dosis: 5 – 10 UI IV
- Según una revisión sistemática la administración de 10 UI de insulina de acción rápida intravenosa resultó comparable con una dosis de 20 UI y con menos asociación a hipoglucemia sintomática.
- Vale la pena resaltar que 1 UI de insulina metaboliza 2.5g de dextrosa.
- Dextrosa:
- Dosis: 25 – 50 g IV.
- Concentración de dextrosa según la presentación disponible:
- DAD 5% de 500ml: 25g
- DAD 10% de 250ml: 25g
- DAD 50% de 50ml: 25g
- La administración debe hacerse concomitante con la insulina.
- Los estudios que han comparado dosis baja de insulina (5 UI) versus dosis estándar (10 UI), no mostraron diferencia en cuanto a la disminución del K+ entre grupos, pero sí era menos común la hipoglucemia en el régimen de dosis baja.
- Debido al riesgo de hipoglucemia, las concentraciones de glucosa en sangre deben ser monitoreadas de cerca.
- Con concentraciones de glucosa >200 mg/dl (11.1 mmol/l), la insulina puede administrarse sin glucosa adicional.
- Agonistas β-adrenérgicos:
- Dosis: 15 – 20 mg.
- Se puede usar como alternativa o adicional a la insulina más dextrosa.
- Es efectiva su administración tanto intravenosa como nebulizada o inhalada.
- Se evidencia disminución significativa de las concentraciones de K+ con un pico máximo a los 120 minutos.
- Se ha demostrado que los efectos del salbutamol junto a la insulina son potencialmente sumativos.
- Bicarbonato de sodio:
- Dosis: 2 mmol/Kg de peso IV en dosis única.
- Activa la bomba Na+ K+ ATPasa y corrige la acidosis metabólica subyacente, lo que lleva a disminución de las concentraciones de sK+.
- Su uso en muchos contextos es ampliamente controversial, incluida la hiperK.
- Se sugiere su uso en pacientes con acidosis metabólica (pH <7.20) y que puedan tolerar dicha carga de sodio.
- También se recomienda, cuando existe de forma concomitante, hiperK e hipoNa.
- Insulina:
🎯Eliminación del K del cuerpo
- Se usan agentes quelantes de K+, la diálisis y los diuréticos de asa.
- Diuréticos de Asa:
- Furosemida a dosis de 1 – 2 mg/kg IV
- Hasta la fecha, no hay estudios que investiguen su eficacia en eliminar el potasio en este contexto.
- Probablemente útiles en pacientes con hiperK con sobrecarga de volumen, como en IC, y potencialmente útiles después de la reanimación de líquidos en otros pacientes.
- Agentes quelantes:
- Datos muy limitados sobre el uso de agentes quelantes de K+ para el manejo de la hiperK aguda.
- Aunque el sulfonato de poliestireno sódico ha sido utilizado durante 60 años, su eficacia no ha sido estudiada en ensayos controlados aleatorizados grandes.
- Se han reportado efectos adversos GI raros.
- No debe administrarse con sorbitol debido a la asociación entre esta combinación y necrosis intestinal.
- Nuevos agentes quelantes:
- Nuevos quelantes de potasio como Patiromer y Ciclosilicato de Zirconio Sódico han sido aprobados recientemente con resultados prometedores en la eliminación de potasio.
- El Ciclosilicato de Zirconio Sódico parece tener un inicio de acción apropiadamente rápido.
- Diálisis:
- La diálisis elimina el K+ de la sangre en pacientes con hiperK.
- Se recomienda una consulta de nefrología en todos los pacientes que se presentan al SU con hiperK y reciben terapia de diálisis.
- Además, los pacientes con hiperK refractaria al tratamiento o hiperK con IRA deben ser referidos a nefrología para considerar la diálisis.
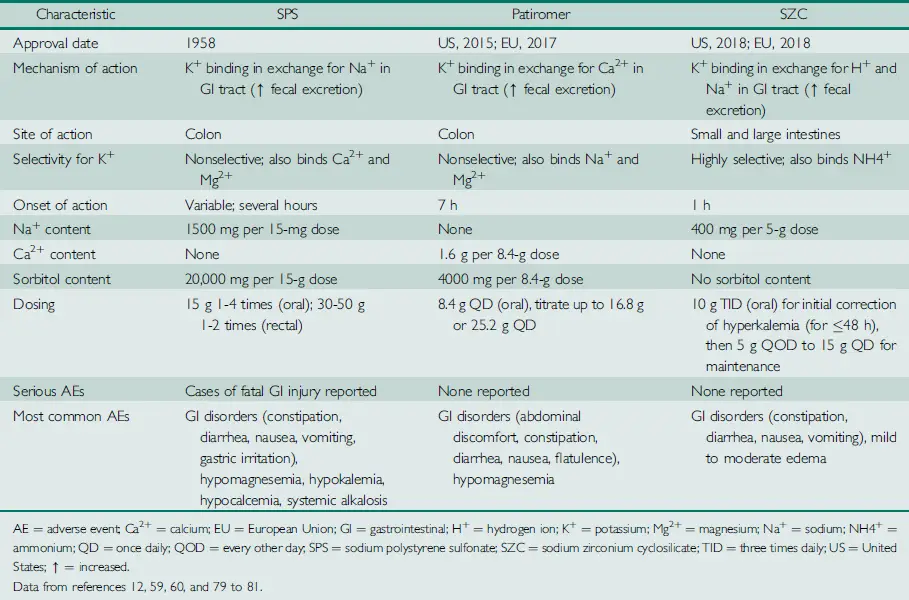
Nuevos agentes quelantes de K+
- Todos los utilizados para el manejo de la hiperK son no absorbibles y consisten en un contraión que se intercambia por K+, facilitando la eliminación del K+ unido en las heces.
- Sulfonato de Poliestireno Sódico (SPS)
- Hasta hace poco era el único conocido disponible.
- Datos clínicos sobre eficacia son limitados.
- Patiromer Sorbitex Calcio (Veltassa) y Ciclosilicato de Zirconio Sodico (SZC; Lokelma, ZS-9)
- Dosis:
- Patiromer: 8.4g al día (max. 25.2g) VO
- SZC: 10g 3 c/8 horas VO en hiperK aguda
- Aprobados en Estados Unidos y Europa
- Los datos clínicos sobre eficacia se han extraído de ensayos clínicos
- Son más palatables que el SPS por lo que aumentan la adherencia
- La guía NICE los recomiendas en hiperK potencialmente mortal
- Se debe usar en conjunto con el cuidado estándar
- En hiperK crónica se debe iniciar la dosis recomendada y luego ajustar según las concentraciones séricas de K+.
- Ambos son costosos, sin embargo en estudios de costo-efectividad se demostró menores costos de hospitalización, mejoría en la supervivencia y aumento de la calidad de vida.
- Dosis:
Re-Evaluación
- La evaluación frecuente de las concentraciones de potasio está indicada en pacientes con hiperK aguda.
- Dado que el inicio de acción de los agentes desplazadores de potasio, como la insulina-glucosa y los agonistas β-adrenérgicos, es de 30–60 minutos, se puede realizar una re-evaluación del K+ a los 60 minutos después de su administración.
- Estos medicamentos no excretan el potasio sino que solo lo trasladan al interior de la célula, esperándose un rebote de hiperK; por lo tanto, la re-evaluación es crucial.
- Puede ocurrir un rebote hacia valores más altos a las 2–3 horas si el K+ no ha sido eliminado del cuerpo durante ese período.
- Los niveles de glucosa (central o periférica) también deben ser monitoreados en pacientes que reciben tratamiento con insulina y dextrosa, debido al riesgo de hipo o hiperglucemia.
- La duración del monitoreo frecuente de la concentración de K+, el monitoreo cardíaco continuo y el monitoreo frecuente de la presión arterial dependerá de la severidad de la hiperK, la gravedad de sus manifestaciones, la probabilidad de rebote y el contexto clínico general del paciente y su respuesta al tratamiento.
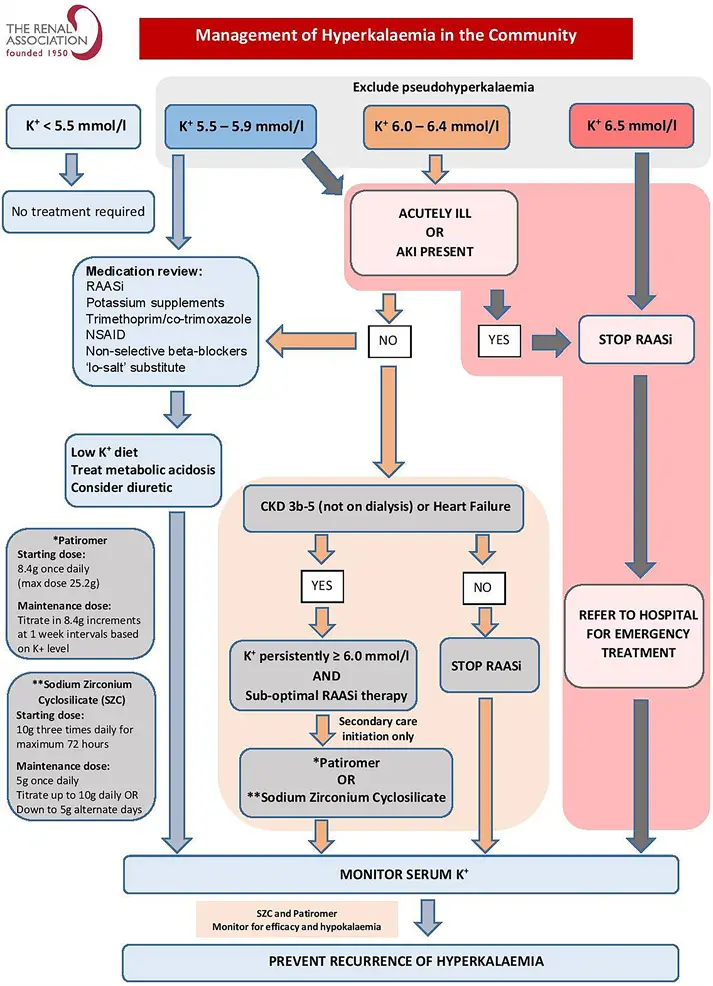
Tratamiento de la hiperK crónica
- HiperK crónica: Episodios recurrentes de concentraciones elevadas de sK que requieren terapia de mantenimiento continua.
- No hay consenso sobre la frecuencia, severidad o duración de estos episodios que definen la cronicidad.
- Más probable de identificarse en individuos con paraclínicos más frecuentes y a menudo es asintomática.
- Recomendaciones para el manejo:
- Uso de diuréticos de asa o tiazídicos.
- Modificación de la dosis de los SRAAi.
- Eliminación de otros medicamentos que causan hiperK.
- Diuréticos:
- Promueven la excreción urinaria de K+ en pacientes con ERC o enfermedad renal diabética (ERD).
- Fludrocortisona:
- Puede aumentar la excreción de K+ pero está asociado con un riesgo aumentado de retención de líquidos, hipertensión y lesión vascular.
- Agentes quelantes aprobados por la FDA:
- Pueden proporcionar beneficios para el manejo de la hiperK crónica evitando las limitaciones de otros tratamientos.
- A tener en cuenta dentro de las limitaciones del manejo a largo plazo:
- Los diuréticos pueden aumentar el riesgo de gota y depleción de volumen, y su efectividad depende de la función renal residual.
- La discontinuación o reducción de la dosis de la terapia con SRAAi puede conducir a resultados adversos cardio-renales.
- Se necesitan iniciativas educativas para aumentar el conocimiento sobre el manejo de la hiperK crónica entre los médicos de atención primaria, internistas y nefrólogos.
Conclusiones
- La hiperK aguda es un problema frecuentemente observado en los servicios de urgencias y uno con consecuencias potencialmente fatales.
- Se recomienda la monitorización de signos vitales y la realización de un ECG de 12 derivaciones en todos los pacientes con una concentración de K+ >6 mmol/l.
- En todos los pacientes con hiperK y presencia de cambios en el ECG, se deben administrar de inmediato sales de calcio.
- Adicionalmente, se deben tomar medidas para trasladar el K+ al compartimento intracelular (es decir, insulina-glucosa, agonistas β-adrenérgicos) y eliminarlo del cuerpo.
- La re-evaluación frecuente de las concentraciones de sK+ es esencial para monitorear el éxito del tratamiento y detectar un aumento de rebote en el K sérico.
- Nunca se olviden de la hiperk crónica, puede llegar a valores críticos y poner en riesgo la vida de los pacientes.